
2020 官网升级中!现在您访问官网的浏览器设备分辨率宽度低于1280px请使用高分辨率宽度访问。
胰蛋白酶是一种丝氨酸蛋白酶,用于降解细胞间结合蛋白从而使细胞脱离其培养介质,令细胞之间相互进行分散。胰蛋白酶大致可以分为两种,一种是传统使用的动物源性的胰蛋白酶,主要提取自牛或猪的胰腺组织;另一种则是非动物源性胰酶,即利用基因重组技术生产的重组胰蛋白酶。
早期的胰蛋白酶是从牛、猪、羊的胰脏中提取,通过多重结晶方式纯化,并进一步采取层析及超滤技术制备而得。该酶易溶于水,不溶于三氯甲烷、乙醇、乙醚等有机溶剂。最初胰蛋白酶在生物制药的主要应用是胰岛素的生产,后期也在疫苗制备、细胞培养领域中应用起来。但动物源的胰蛋白酶具有极大的潜在风险,其自身可能携带大量可感染人的病毒,例如:疯牛病的牛带有的BSE病毒,猪的口蹄疫病毒,可在人和动物之间传播的禽类流感病毒等。
.jpg)
这样的情况可不少:上世纪60年代于脊髓灰质炎疫苗中检测到SV40病毒,在减毒黄热活疫苗中发现禽白血病病毒。2010年,Merck和GSK公司已上市的轮状病毒疫苗中又先后检测到猪圆环病毒核酸序列。据当时科学家推测,导致这种情况的“元凶”可能是疫苗生产所必需的细胞在增殖的过程中所用的猪胰蛋白酶造成。因此,如何提高生物制品的安全性成为了监管层的关注重点。
2019年9月国家药监局发布了《疫苗上市后生产工艺变更研究技术指导原则》(征求意见稿):“生产过程中,应尽可能避免使用人源或动物源性原材料”,疫苗生产原辅料变更,将动物源性的牛血清或胰酶变更为无动物源的原辅料,只需要通过简化变更流程,鼓励企业进行无动物源原辅料的变更。2020年版《中国药典》也增加了重组胰蛋白酶标准。
.jpg)
重组胰蛋白酶的氨基酸序列与动物源提取的胰蛋白酶完全一致,该酶包含两种胰蛋白酶活性形式:α-胰蛋白酶和β-胰蛋白酶。其活性受丝氨酸蛋白酶抑制剂如PMSF和TLCK等、金属离子螯合剂如EDTA等的抑制。在应用上,可替代传统胰蛋白酶用于疫苗、干细胞、免疫细胞治疗、胰岛素生产等对动物来源材料有严格限制的生物制药产业。
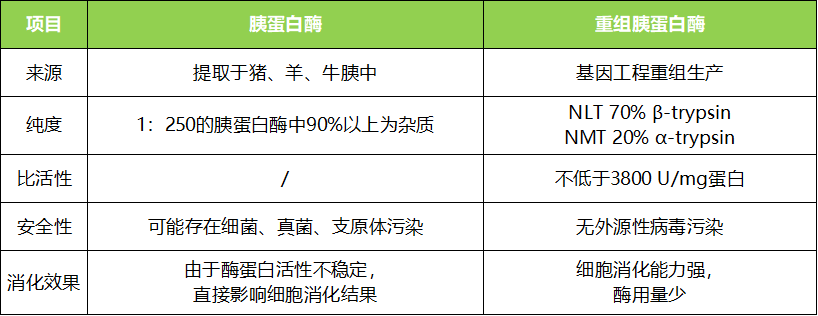
药典级别的重组胰蛋白酶要求微生物的菌落总数不超过100cfu/mL,宿主蛋白质残留量不超过0.01%,外源性DNA残留量不超过10ng/mg。由上表可以看出,相比传统动物源提取的胰蛋白酶,重组胰蛋白酶在活性、纯度以及无动物源性等方面优势更为明显,更符合生物制药行业发展趋势。
在疫苗细胞基质制备中胰蛋白酶是常用的原料,而动物源性胰蛋白酶内一些能引起人畜共患病的潜在病毒都有可能带入终产品中。
.jpg)
随着SARS,H1N1,禽流感等病毒影响下,为了减少已知污染物和未知污染,相关法规已有明确要求,如在药物标签上注明是否应用动物源的原料,生物制药公司促使原料生产商在选择原料的时候提高对AOF的关注度;所有用血液和血浆来源的药物制品在标签上注明:警告病毒和阮病毒疾病传播的风险。
作为制药辅料的用酶—制订新版重组酶的标准将包括胰蛋白酶、胃蛋白酶,木瓜蛋白酶,胶原酶等,其中第一个给出标准的就是重组胰蛋白酶。
↑ 点击图片了解产品详情
新葡的京集团3512vip重组胰蛋白酶是由微生物基因重组表达生产,氨基酸序列与猪胰腺来源的胰蛋白酶完全一致,且具有与动物源性猪胰蛋白酶相同的酶学性质,可替代猪胰腺来源胰蛋白酶应用于各种生物技术过程中,如:重组胰岛素生产、细胞培养、细胞发酵、蛋白质的酶解以及各种组织的细胞分离等。胰蛋白酶活性受丝氨酸蛋白酶抑制剂如PMSF等的抑制,金属离子螯合剂如EDTA等也能抑制酶活。
1.产品纯度:
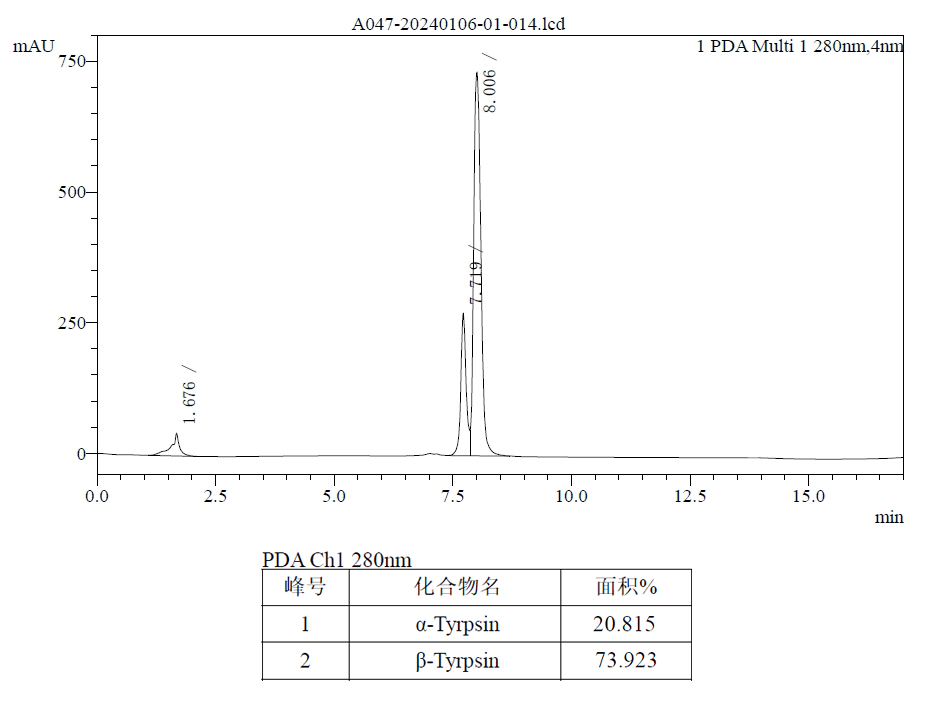
结论:检测结果分析,β-Trypsin的含量可达70%以上,符合2020版中国药典标准。
2.冻融稳定性测试
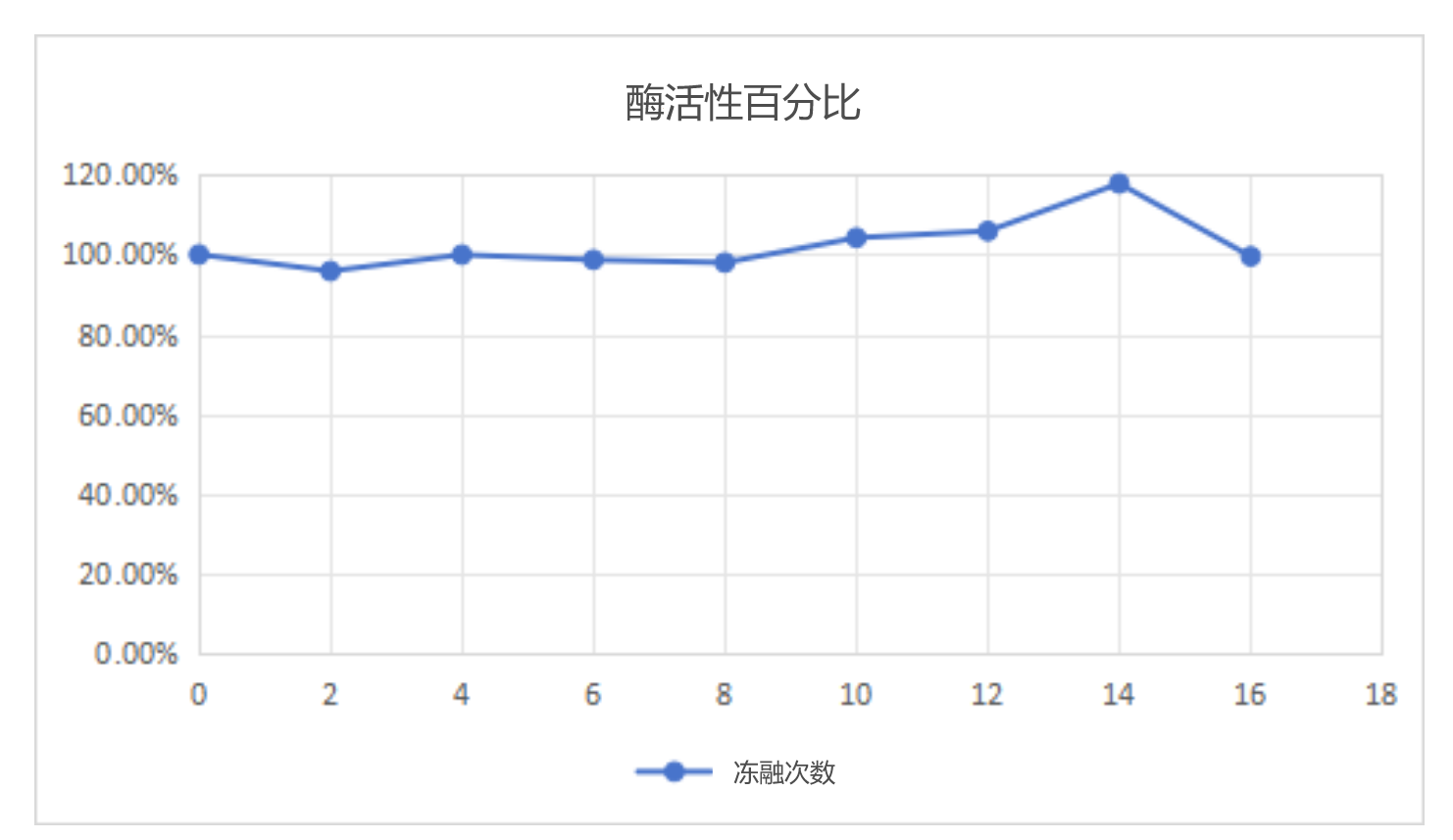
结论:产品分别在经过不同次数冻融后均未观察到酶活性损失。
3.温度稳定性测试
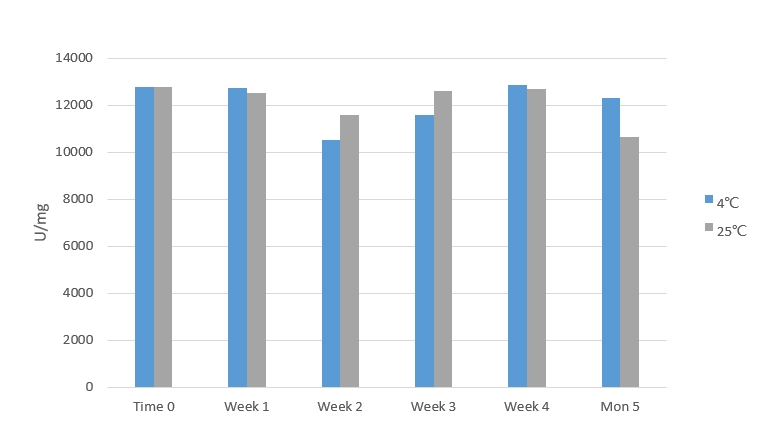
结论:产品在4℃或室温避光条件下4周内活性未降低;在4℃条件下5个月内活性未降低。